2016年9月30日,国际学术期刊Journal of Biological Chemistry在线发表了中国科学院上海生命科学研究院生物化学与细胞生物学研究所王恩多研究组最新研究成果:“Translational Quality Control by Bacterial Threonyl-tRNASynthetases”。
蛋白质合成中,氨基酰-tRNA合成酶(AARS)从源头上介导氨基酸与tRNA之间的精确匹配,生成正确的氨基酰-tRNA,为核糖体提供原料。一方面,AARS需要高效地催化氨基酰化反应以合成正确的氨基酰-tRNA,满足蛋白质合成;另一方面,AARS需要通过水解编校功能以确保氨基酸与tRNA的正确匹配。
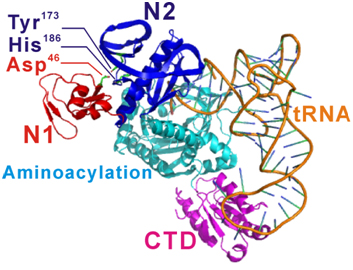
苏氨酰-tRNA合成酶(ThrRS)属于经典的具有编校功能的AARS,包含N1结构域(功能未知)、N2编校结构域、氨基酰化结构域与RNA结合结构域。N1结构域在氨基酰化、编校反应中的功能一直未知。在王恩多研究员的指导下,副研究员周小龙及博士研究生陈云等通过基因组数据分析鉴定了细菌来源的多种ThrRS在N1结构域的存在与N2结构域活性位点的分布上的多样性与复杂性。通过体内与体外实验证明了多种细菌类ThrRS介导的蛋白质合成质量控制机制,揭示了发生在细菌类ThrRS N2结构域的编校功能依赖于N2与N1结构域间的通讯机制。进一步的,鉴定了N1与N2结构域中调控结构域间通讯的氨基酸残基与发挥作用的途径。该研究阐明了ThrRS N1结构域在遗传信息精确性传递中的关键作用及其发挥作用的分子机制;如果破坏N1-N2结构域的通讯机制产生错误翻译(mistranslation),则导致细菌与微生物死亡。
该项研究获得国家科技部基础研究基金、国家自然科学基金、中科院及其青年创新促进会、上海市启明星计划的经费资助。