2016年12月12日,国际学术期刊Proc Natl Acad Sci USA在线发表了中国科学院上海生命科学研究院生物化学与细胞生物学研究所刘小龙研究组的最新研究成果“Uhrf1 controls the self-renewal versus differentiation of hematopoietic stem cells by epigenetically regulating the cell division modes”。该成果揭示了表观遗传调控因子Uhrf1调控造血干细胞自我更新和分化的分子机制。
造血干细胞对自我更新和分化能力的调节对维持整个造血系统的发育和稳态具有极其重要的作用。造血干细胞对自我更新和分化的调控通过细胞分裂模式来实现。根据分裂之后产生的子代细胞类型的不同,可以将造血干细胞的分裂模式分为:对称的自我更新的分裂(产生两个相同的干细胞)、不对称的分裂(产生一个干细胞和一个分化的子代细胞)和对称的分化分裂(产生两个相同的分化的子代细胞)。调控细胞分裂的分子机制一直以来是发育生物学以及干细胞生物学研究的热点。尽管科学家已经揭示了一些转录因子在调节造血干细胞分裂模式的作用,但表观遗传和分裂模式调控的关系尚不明确。
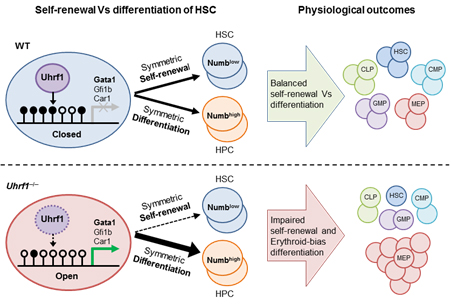
在刘小龙研究员的指导下,博士研究生赵静尧、博士后陈旭峰等人研究发现表观遗传调控因子Uhrf1对造血系统的发育和维持是必需的。在小鼠体内胚胎时期的造血血统特异性敲除Uhrf1造成造血干细胞库耗竭,机体造血失败最终造成小鼠围产期的死亡。Uhrf1缺失的造血干细胞虽然具有正常的生存和增殖能力,但由于进行以牺牲自我更新能力的分化因而很快耗竭了造血干细胞库。细胞分裂模式的分析表明Uhrf1缺失造成造血干细胞更多地进行对称的分化分裂,从而不能建立造血干细胞库。对其下游分化的子代前体细胞进行分析发现Uhrf1缺失的造血干细胞的分化有明显的红系偏好性。RNA-seq和BS-seq分析表明Uhrf1缺失的造血干细胞未能维持红系相关基因的甲基化模式,提前表达了红系相关基因,进而更多的进行了以牺牲自我更新能力的红系偏好性的对称分化模式。在小鼠成体时期的造血系统中敲除Uhrf1同样造成这样的结果,表明Uhrf1控制的这种生理功能维持造血系统的稳态。除此之外,在造血干细胞中过表达红系分化的转录因子Gata1也造成造血干细胞进行更多的对称的分化分裂模式,进而耗竭了造血干细胞。综上所述,我们的研究表明Uhrf1以表观遗传的形式调节造血干细胞的分裂模式,继而控制造血干细胞的自我更新和分化,从而维持造血系统的正常发育和稳态。
该项研究工作得到了生化细胞所公共技术服务中心动物实验技术平台、细胞生物学平台和分子生物学平台的支持。该工作得到了国家科技部(973课题)、中科院先导B项目、国家自然科学基金委,中国博士后基金的经费支持。