周斌研究组揭示心脏修复再生中新血管形成的机制
来源:
时间:2017-06-28
6月26日,国际学术期刊
Journal of Clinical Investigation 在线发表了中国科学院生物化学与细胞生物学研究所周斌研究组的科研成果“Preexisting coronary endothelial cells mediate cardiac neovascularization after injury”。该研究利用系统的遗传谱系
示踪技术揭示了成体心脏修复再生中新生血管的来源,为临床治疗心梗后的心脏再生治疗提供了重要的理论基础和新的思路。
冠状动脉疾病是当今世界上的首要致死疾病,冠状动脉粥样硬化及心肌梗塞等冠状动脉疾病发生后,导致了心脏供血供氧的不足,大量细胞死亡,从而诱发了炎症及损伤修复反应,促使新血管的形成,以恢复损伤区的血液供应,因此,快速的血管新生过程对于心肌损伤后的修复过程具有至关重要的作用。
有关成体心脏损伤后新生血管的起源,目前有三种假说:第一种是血管内皮细胞的自我增殖,第二种是其它类型的末端分化细胞转分化形成血管内皮细胞,第三种是干细胞分化形成血管内皮细胞。成体心脏损伤后,血管内皮细胞会发生自我复制增殖过程,然而是否有干细胞或其他类型的细胞通过细胞分化或转分化作用形成血管内皮细胞仍然存在争议。有研究报道,成纤维细胞在小鼠缺血再灌注损伤模型中发生了间充质细胞向血管内皮细胞的转变(mesenchymal-to-endothelial transition, MEndoT)过程,形成了新的血管内皮细胞。此外,也有研究指出,c-Kit和Sca1阳性的干细胞在成体心脏损伤后具有分化成为血管内皮细胞的能力,不过这些研究结果都有待进一步的证实。
为了系统解决成体心脏损伤后新生血管的来源问题,周斌研究组博士后何灵娟等研究人员建立了6组成纤维细胞转基因或基因敲入小鼠的遗传谱系示踪实验,通过将上述小鼠分别与报告基因小鼠tdTomato交配来追踪成纤维细胞和间充质细胞在成体心脏损伤过程中的细胞命运,结果并没有发现tdTomato阳性的血管内皮细胞,说明成体心脏中成纤维细胞并不具有转分化形成血管内皮细胞的能力。为了进一步研究是否有除了血管内皮细胞以外的所有其它类型细胞能够在成体心脏损伤后形成血管内皮细胞,研究人员又建立了3种血管内皮细胞的遗传谱系示踪实验,通过将血管内皮细胞特异性表达CreER的小鼠与报告基因小鼠交配,在损伤前标记上大部分血管内皮细胞,然后观察损伤后血管内皮细胞的标记百分比是否降低,如果标记百分比没有发生变化,说明新生的血管内皮细胞来源于原来已存在的血管内皮细胞的自我增殖过程,如果标记的百分比降低了,则说明存在其它类型细胞转分化成为血管内皮细胞。结果显示,损伤后,血管内皮细胞的标记百分比没有发生变化,即没有发生其他类型的细胞向血管内皮细胞的转分化过程。上述实验结果说明,在成体心脏损伤过程中,新生血管主要来自于血管内皮细胞的自我复制增殖过程。
该研究得到了美国辛辛那提儿童医院医学中心Jeffery Molkentin教授、香港中文大学吕爱兰教授、北京生命科学研究所陈婷教授、英国伦敦国王学院的徐清波教授、阜外医院的胡盛寿及聂宇教授等大力帮助,并得到了中科院、基金委、科技部以及上海科委等经费支持。
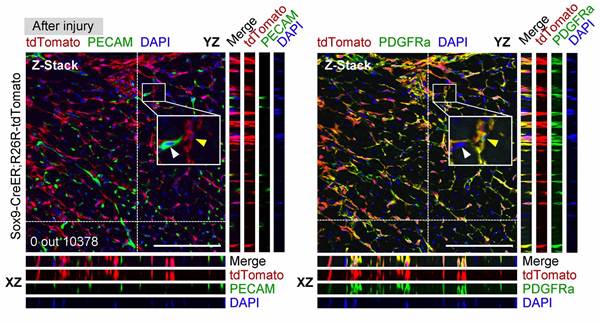
成体心脏损伤后被tdTomato标记的PDGFRa阳性成纤维细胞不会转分化成为PECAM阳性的血管内皮细胞