周兆才研究组揭示胃癌发生过程中抗病毒通路与Hippo-YAP通路互作的分子机制
来源:
时间:2018-01-19
1月16日,国际学术期刊The Journal of Experimental Medicine在线发表中国科学院分子细胞科学卓越创新中心/生物化学与细胞生物学研究所周兆才研究组的最新研究成果“Targeting IRF3 as a YAP Agonist Therapy against Gastric Cancer”。在该项工作中,研究人员揭示抗病毒信号通路对Hippo信号通路的调控作用,特别是IRF3增强YAP活性的调控机制,并发现IRF3可作为YAP高表达型胃癌的治疗靶标,为探索胃癌的病变机理以及相关药物筛选和诊疗策略研发提供基础。
Hippo信号通路在生物个体发育特别是组织器官大小调控过程中具有关键功能,同时在肿瘤发生及免疫应答过程中发挥十分重要的作用。周兆才研究组长期致力于研究肿瘤发生及免疫应答的分子细胞信号机制,近期一系列工作揭示了Hippo、TLR等信号通路在胃肠道恶性肿瘤及炎症免疫应答中的机制与功能,发现了多个新的疾病诊疗标识物及药物靶标(Oncogene 2017; Nature Communications 2017; Nature Immunology 2015; EMBO Journal 2015; Cancer Cell 2014; Cell Research 2014)。
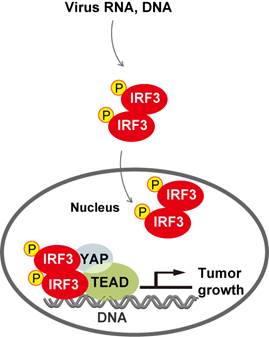
在该项工作中,研究人员通过对胃癌病人临床样本的深入分析,明确IRF3表达在肿瘤中呈现显著上调趋势,并与YAP的表达明显正相关。进一步结合ChIP-Seq和RNA-Seq等研究手段,发现病毒刺激能够显著促进YAP活性及下游基因的转录。机制上,IRF3磷酸化入核之后,可以与YAP和TEAD形成复合物,维持核内YAP蛋白水平,稳定YAP-TEAD与靶基因的结合,促进胃癌细胞增殖(如下图)。细胞和小鼠胃癌模型表明,敲除IRF3或利用小分子化合物抑制IRF3活性,能够阻滞YAP驱动的胃癌生长。这些发现揭示了病毒感染与肿瘤复杂互作的新型分子机制,明确了抗病毒关键分子IRF3与肿瘤增殖关键分子YAP之间的病理相关性,提示IRF3可以作为一个新的药物靶点,为高YAP水平的胃癌及其它恶性肿瘤治疗提供新的思路。