李振斐研究组及合作实验室揭示前列腺癌中雄激素代谢酶17βHSD2的功能及调节机制
来源:
时间:2018-09-27
9月18日,国际学术期刊Clinical Cancer Research在线发表了中国科学院生物化学与细胞生物学研究所李振斐研究组的最新研究成果“Functional silencing of HSD17B2 in prostate cancer promotes disease progression”。
前列腺癌的发生发展与雄激素密切相关。因此,参与雄激素合成的类固醇代谢酶是前列腺癌临床治疗的重要靶点。17βHSD2是雄激素合成过程中重要的类固醇代谢酶。该代谢酶催化了甾体第17位羟基向酮基的转化。17位羟基对于雄激素活性有重要影响,17位酮基会让雄激素丧失活性。17βHSD2通过对该位点的调控,精细地调节了体内活性形式的雄激素浓度。但该类酶与前列腺癌的进展及其相关调控机制,尚未明确。
李振斐研究组致力于研究类固醇激素代谢与前列腺癌治疗,通过对类固醇代谢关键酶以及靶向药物的探索并结合临床实验,探索前列腺癌临床诊治的新生物标志物和治疗靶点。该团队发现类固醇代谢酶17βHSD2的表达随前列腺癌的进展逐步降低。17βHSD2将睾酮(testosterone,T)和二氢睾酮(dihydrotestosterone, DHT)代谢成它们的前体小分子来减少体内活性形式的雄激素浓度。进一步体内外实验证实,上调17βHSD2的表达能够抑制雄激素诱导的细胞增殖和异位瘤生长。深入研究后他们发现17βHSD2的表达水平受DNA甲基化、雄激素的应激以及mRNA可变剪接的调控。有意思的是,受到剪切因子SRSF1和SRSF5的调控,17βHSD2能够产生两个新的剪切体。这两个新的剪切体失去了催化活性,并且可以通过与全长的17βHSD2相互作用促进其降解。
该研究由李振斐研究团队,同济大学附属同济医院吴登龙研究团队和克利夫兰诊所Nima Sharifi研究团队合作完成。该工作获得了国家科技部重点研发计划、中科院战略性科技先导专项、国家自然科学基金、中科院青年创新促进会、美国前列腺癌基金会和国家癌症研究所资助。感谢蛋白质科学设施(上海)张江实验室质谱平台、生化与细胞所公共技术服务中心和动物平台的支持。
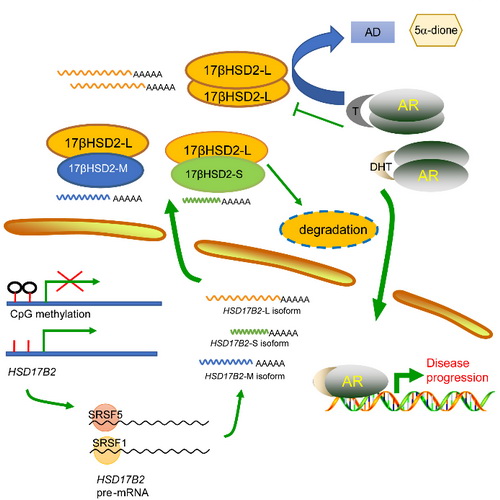
DNA甲基化、雄激素应激和mRNA的可变剪接都可使HSD17B2功能性沉默
