周斌研究组揭示成体Sca1+心脏干细胞的分化潜能
来源:
时间:2018-12-20
冠状动脉疾病引起心肌梗死和心衰,是人类因疾病死亡的首要原因。发生急性心肌梗死后,心肌细胞和血管内皮细胞大量死亡,仅少量心肌细胞分裂增殖,如何提高心脏心肌细胞的再生已经成为该领域的研究热点。前期研究表明在心脏中存在的心脏干细胞可以在损伤的情况下贡献到心肌细胞,从而提高损伤心脏的修复能力。其中,体外细胞和移植实验表明Sca1+心脏干细胞可以转分化为心肌细胞,同时Sca1+作为血管干细胞可以通过增殖、分化转变为血管内皮细胞。综上,Sca1+具有多种分化潜能,但心脏中内源性的Sca1+细胞能否贡献到心肌细胞和内皮细胞有待于进一步研究。
为了系统研究成体Sca1+心脏干细胞在正常生理和心脏损伤情况下的命运变化,研究人员建立了特异性标记Sca1+心脏干细胞的谱系示踪系统,抗雌激素药物他莫昔芬(tamoxifen)诱导处理24-48小时后,收集样本检测发现Sca1-2A-CreER;R26-tdTomato小鼠可以特异和高效地标记Sca1+心脏干细胞,其中主要标记血管内皮细胞和少量的成纤维细胞。利用这个特异性的小鼠,研究人员分别在生理情况以及心肌梗死情况下检测了Sca1+心脏干细胞的转分化情况。通过对8周Sca1-2A-CreER;R26-tdTomato小鼠注射tamoxifen,收集注射后1-12周小鼠心脏样本,检测发现稳态心脏中,Sca1+心脏干细胞可以贡献到心脏内皮细胞和少量的成纤维细胞,但并不能转分化心肌细胞。进一步实验中,研究人员在tamoxifen诱导的Sca1-2A-CreER;R26-tdTomato小鼠中进行了心脏损伤模型,包括心肌梗死,心脏缺血再灌注等模型。研究人员发现在心脏损伤模型中,Sca1+心脏干细胞可以贡献为血管内皮细胞和成纤维细胞,而并不转分化为心肌细胞。以上结果说明,成体Sca1+心脏干细胞具有转分化为血管内皮细胞和成纤维细胞的潜能,通过血管新生促进心脏修复。杂志同期刊发了哈佛大学医学院Richard T. Lee教授对于该项工作及同期Sca1干细胞相关工作的专题评论,他认为该工作揭示了成体哺乳动物中Sca1心脏干细胞的命运,推动了心脏干细胞领域的发展和进步。
该项工作在周斌研究员的指导下,由博士后唐娟等完成,得到了中国医学科学院聂宇教授、阜外医院胡盛寿教授、香港中文大学吕爱兰教授及阿斯利康的Qing-Dong Wang研究员等的大力支持,同时得到中国科学院、国家基金委、国家科技部、上海市科委等资助。
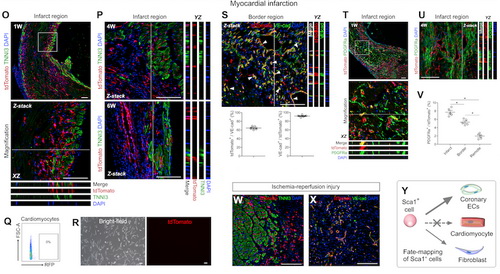
Sca1+心脏干细胞在心肌梗死损伤模型(O-V)以及心肌缺血再灌注模型中(W-X)中不能转分化为心肌细胞. 在心脏稳态和损伤情况下,Sca1+ 心脏干细胞具有转变为内皮细胞和成纤维细胞的潜能,但不能转化为心肌细胞(Y).
