程红研究组揭示出核受体NXF1协同调控转录延伸、可变加尾及出核的新机制
来源:
时间:2019-05-18
2月25日,国际知名学术期刊Molecular Cell在线发表了中国科学院生物化学与细胞生物学研究所程红研究组的最新研究成果“The mRNA export receptor NXF1 coordinates transcriptional dynamics, alternative polyadenylation and mRNA export”,报道了mRNA出核因子调控可变加尾的重要功能和普遍规律,并揭示mRNA出核受体NXF1通过协同调控转录延伸、可变加尾和mRNA出核转运过程,在基因表达过程中起中心枢纽作用。
真核基因表达是一个复杂的多步骤过程,包括转录、pre-mRNA的加工、核质转运、翻译和mRNA的降解等,这些步骤通常偶联在一起从而确保遗传信息的精确传递。绝大多数pre-mRNA的3'端需要经过切割和多聚腺苷酸化,产生具有多聚腺苷酸尾的成熟mRNA。哺乳动物基因通常含有多个多聚腺苷酸位点(PAS),这些PAS的选择性使用可产生具有不同长度的3'非翻译区(3'UTR)、甚至不同编码序列的异构体(这一过程称为可变加尾)。可变加尾是近年备受关注的一种重要的转录后调控方式,在分化发育、肿瘤发生等多个生理病理过程中发挥重要调控功能。可变加尾受到多种因素的影响,近年来的研究提示mRNA出核转运可能参与调控可变加尾,但关于mRNA出核转运因子调控可变加尾的普遍规律与分子机制目前还不清楚。
程红研究组长期从事RNA转运与降解的功能机制研究,近年获得一系列进展(
EMBO J 2017;
Nucleic Acids Res 2017;
J Cell Biol 2018; Nucleic Acids Res 2018)。基于mRNA出核接头蛋白ALYREF结合在mRNA 3'区域的发现(
Nucleic Acids Res 2017),研究人员推测mRNA出核因子可能参与调控可变加尾。利用3'端测序技术(3'READS),研究人员发现mRNA出核受体NXF1和mRNA出核复合体TREX组分(包括ALYREF)均能不同程度地促进远端PAS的使用,产生具有长3'UTR的异构体,其中NXF1的作用最为明显。通过系统分析3'READS数据,研究人员发现两种全新影响可变加尾的基因特征:基因长度及3'外显子的AT丰度。进一步机制探索发现,NXF1通过结合在活跃转录的基因上并与
RNA聚合酶II互作,显著促进RNA聚合酶II在基因3'端的延伸,这与其辅助远端PAS使用的功能高度吻合。有趣的是,在成熟mRNA上,NXF1通过与CFI(Cleavage Factor I)互作,结合富含UGUA元件的长
3'UTR异构体,并促进其出核转运。该工作提示mRNA出核转运不仅受转录和加工等基因表达通路上游步骤的影响,还可依赖出核因子与转录和RNA加工机器的相互作用逆向调控上游步骤,这种逆调控可能对遗传信息的精准传递十分关键。
该研究工作由程红研究组和Rutgers New Jersey Medical School的田斌教授实验室合作完成,程红研究组的博士生陈素丽和张衡以及田斌实验室的博士后王睿甲和郑定海是本文的共同第一作者。该工作获得科技部、中科院、自然科学基金委等经费资助,同时得到生化与细胞所细胞分析技术平台、分子生物学技术平台等的大力支持。
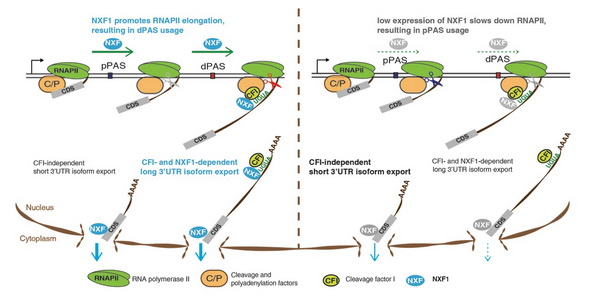
NXF1协同调控转录延伸、可变加尾和mRNA出核转运的模式图
在正常状态下,NXF1辅助RNA聚合酶II的转录延伸,促进远端PAS被优先使用,产生长3’UTR异构体;NXF1与CFI-68协同作用辅助长3’UTR异构体的出核转运。当NXF1水平较低时,转录延伸变慢,导致近端PAS被优先使用,产生短3’UTR的异构体;短3’UTR异构体的出核转运对NXF1和CFI-68的表达水平相对不敏感。
