胡荣贵研究组揭示泛素化信号调节细胞选择性自噬的分子机制
来源:
时间:2020-03-18
7月14日(当地时间),国际学术期刊 Cancer Cell 在线发表了中国科学院上海生命科学研究院生物化学与细胞生物学研究所胡荣贵课题组的最新研究成果,研究发现具有肿瘤抑制活性的泛素连接酶HACE1,通过介导细胞自噬受体蛋白Optineurin (OPTN)的泛素化修饰,促进细胞自噬受体复合物形成,“激活”细胞自噬,从而抑制肿瘤细胞增殖的分子机制。
自噬 (Autophagy) 途径是细胞对胞内的大分子物质的包被、吞噬后在溶酶体中降解的过程。自噬最早被认为是非选择性的,而近期研究发现由于自噬受体蛋白的存在而对自噬底物的进行分选、运输而选择性的靶向后者的降解,从而赋予依赖自噬降解的蛋白质稳态极其精密的动态调控。目前已知的蛋白质受体蛋白如p62/SQSTM1、OPTN等有约十种左右。已知这些自噬受体蛋白的基因突变或缺失与多种人类疾病相关。这些疾病表现各异却也有部分共同的特点。OPTN由于其基因的某些位点的突变最早被发现与与人类的各型青光眼有关而得名。近来,OPTN的另一些基因位点的突变被发现与肌萎缩侧索性硬化症(ALS) 或Paget’s 骨系统疾病有关。已知OPTN 蛋白参与调节细胞内重要的免疫信号通路、细胞极性及细胞自噬等,但其机理尚不清楚。关于这些自噬受体蛋白本身的修饰及功能调控,以及自噬受体蛋白之间的相互作用及其组织方式(如是否和如何形成复合物)等目前了解还很初步,而成为当前自噬领域的研究热点之一。
博士生刘征兆、陈朋、中山医院高虹博士等发现具有肿瘤抑制活性的泛素连接酶HACE1能够与 OPTN 蛋白直接相互作用,并催化OPTN的多泛素化,被泛素化的OPTN被 p62 的泛素结合结构域识别并形成大的自噬受体蛋白复合物,显著增加细胞内自噬途径降解蛋白质的通量从而“激活”细胞自噬。这提示细胞内泛素化信号系统调节细胞选择性自噬的一种新的模式。有趣的是,OPTN蛋白经HACE1介导的以泛素K48方式连接的泛素链修饰后主要通过溶酶体依赖的自噬途径被降解。这个发现不同于”泛素K48连接的多泛素链只靶向底物进入蛋白酶体降解”的经典知识。基于大量临床样本的数据进一步表明,HACE1和OPTN在肝癌、胃癌等肿瘤组织中的高发突变或低表达。而在多种肿瘤细胞中恢复HACE1-OPTN轴心可以激活自噬而显著抑制肿瘤增殖。 HACE1-OPTN功能缺陷导致其调控的自噬底物累积,这些累积的底物可能成为相关肿瘤分型的分子标志物。本项进展为进一步研究OPTN的生理作用以及其突变的病理意义提供了新的研究视角,也可能有助于以细胞自噬为靶向的肿瘤抑制药物开发。
本项工作的完成过程中,得到了国内外多个课题组重要的的支持和帮助:哈佛医学院的Daniel Finley教授,中科院上海生化与细胞所季红斌、阮康成、李林等实验室、复旦大学附属中山医院孙一红、陈世耀、邹健实验室、安徽医科大学刘晓颖、范礼斌实验室、第二军医大学程树群教授、东京都医学科学研究所的Masaaki Komatsu教授、新泽西癌症研究所的Eileen White教授等。中科院上海生化与细胞所的曾嵘、李青润、惠利健、李党生研究员、法兰克福生化所的Ivan Dikic教授、美国国立研究所的刘正刚教授、耶鲁大学的吴殿青教授等也提供了非常有益的建议和帮助。该项研究工作得到了国家科技部、国家自然科学基金委、徐汇中心医院癌症研究中心、中科院神经所开放课题、中科院重大仪器研发专项等经费支持。
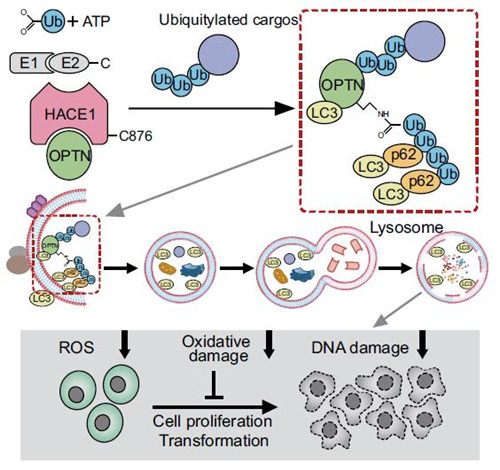
HACE1泛素化自噬受体蛋白OPTN激活细胞自噬抑制肿瘤的分子机制示意图 :泛素连接酶HACE1介导自噬受体OPTN的泛素化,促进OPTN与 p62 的相互作用,并形成大的自噬受体蛋白复合物,显著增加细胞内自噬途径降解被氧化损伤的蛋白质的通量,从而“激活”细胞自噬、抑制肿瘤增殖。