孟飞龙研究组发现哺乳动物细胞内调控DNA重组方向性的关键因子
来源:
时间:2020-05-15
4月30日,国际学术期刊Cell Research在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)孟飞龙研究组的研究论文“ERCC6L2 promotes DNA orientation-specific recombination in mammalian cells”。该研究利用B细胞抗体类型转换重组为模型,发现ERCC6L2蛋白决定了抗体类型转换中DNA重组方向特异性。
在适应性免疫中,免疫受体基因在免疫细胞发育的特定时期,会主动地发生DNA损伤。这种程序性DNA损伤需要被高效地修复,才能在DNA损伤发生时仍维持细胞的免疫学功能。抗体类型转换就是一个很好的例子:在抗体类型转换中,脱氨酶AID在抗体恒定区基因上产生的两个DNA双链断裂(DSBs)总是倾向于以“中间片段删除”的方式连接(附图中1-4连接),最后重组成具有功能的抗体基因。在哺乳动物细胞中其它原因产生的DNA断裂连接,并不具备这种方向倾向性,即“中间片段删除”和“中间片段反转”的比例为1:1。这种哺乳动物细胞中方向倾向性重组的分子机制仍然未知。
在该项研究中,研究人员首次高通量整合了CRISPR/Cas9遗传学筛选与化学遗传学方法,对DNA修复基因在不同种类DNA损伤小分子化合物处理中的作用,做了全景描述。发现了新的非同源末端连接因子,并对于其中含有SWI2/SNF2家族重构酶/转座酶催化活性结构域的ERCC6L2基因进行了深入研究。与经典的非同源末端连接因子类似,ERCC6L2基因突变的病人呈现出骨髓衰竭的病征。在哺乳动物细胞体系中,ERCC6L2基因缺陷的细胞特异性对DNA双链损伤敏感,而ERCC6L2基因缺陷的B细胞不能进行高效的抗体类型转换。对于B细胞免疫功能的进一步测定,研究人员发现ERCC6L2单基因缺陷影响了抗体类型转换,并不影响前体B细胞内的V(D)J免疫重排或生发中心B细胞内的抗体高频突变。在DNA损伤发生后,ERCC6L2蛋白能够通过其C端结构域,迅速地被招募到DNA损伤位点。而其N端重构酶/转座酶催化活性结构域是其发挥功能所必需的。ERCC6L2蛋白影响了其它非同源末端连接因子,特别是DNA连接酶复合物的招募。这种缓慢发生的末端连接,导致了染色质三维结构域内DNA断裂的快速处理,从而使整个DNA重组体系丧失了方向特异性信息。利用高通量全基因组染色质易位测序法(HTGTS),研究人员发现ERCC6L2蛋白酶活是方向倾向性重组必需的。该研究发现ERCC6L2是一个新的非同源末端连接因子,可以通过调控DNA末端连接的方向性促进DNA重组。这些发现拓展了DSBs损伤修复领域的认知,发现了抗体类型转换重组过程中方向特异性连接的决定因子。对于方向性DNA重组的分子机制,仍有待进一步的研究。
分子细胞卓越中心孟飞龙研究员为本文通讯作者,哈佛大学医学院刘小乐教授为共同资深作者。研究组的博士后刘晓静及博士研究生刘婷婷、尚雅芳、代鹏飞为本文共同第一作者。该研究还得到了NIH癌症研究中心的Rafael Casellas研究员、哥伦比亚大学的查珊教授、上海交通大学的Leng-Siew Yeap教授、北京大学的胡家志教授、中山大学的董俊超教授、分子细胞卓越中心周波研究员、上海师范大学的郑小琪教授等的大力协助。该研究得到了国家重点研发计划项目、中国科学院战略性先导科技专项、国家自然科学基金、中国博士后科学基金等的经费支持,以及分子细胞中心GTP研究中心、动物实验技术平台、细胞分析技术平台和分子生物学平台等的大力支持。
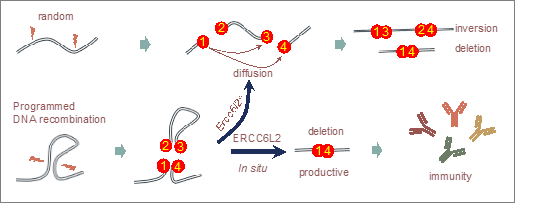
ERCC6L2决定抗体类型转换重组中DNA末端连接的方向性
