1月13日,国际学术期刊EMBO Molecular Medicine在线发表中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)季红斌研究组与同济大学附属肺科医院张鹏研究组的合作论文“Nanog maintains stemness of Lkb1-deficient lung adenocarcinoma and prevents gastric differentiation”。该研究建立了一个粘液型肺腺癌的小鼠模型并揭示其发病机制,发现该肺癌亚型与耐药密切相关,并提出联合治疗的干预策略,为这一特殊肺癌类型的临床诊治提供了新思路。
近年来研究发现,肿瘤谱系转变往往会导致靶向治疗耐药。粘液型腺癌被认为由肺腺癌发生胃上皮细胞谱系转变而来的。目前关于肺腺癌向胃上皮细胞谱系转变的机制及其对治疗反应的影响还不甚清楚。研究人员发现,来源于KrasLSL-G12D/+;Lkb1flox/flox(KL)小鼠模型的肺腺癌具有高度可塑性,而且特异性表达干性基因Nanog。在KL模型中敲除Nanog会诱导肺腺癌向胃上皮细胞谱系发生转变,并导致这些粘液型肺腺癌对苯乙双胍表现出明显的治疗抵抗。这种转变主要涉及Notch信号通路的激活,而γ分泌酶抑制剂能够显著抑制肺腺癌向胃上皮细胞谱系的转变。进一步研究表明,联合苯乙双胍和γ分泌酶抑制剂可以有效抑制粘液型肺腺癌的恶性进展。
该研究建立一个新的粘液型肺腺癌小鼠模型,揭示Notch信号通路在肺腺癌向胃上皮细胞谱系转变中的功能,发现粘液型肺腺癌的耐药性并提出新的治疗干预策略,为深入理解粘液型肺腺癌的发病机制奠定坚实的理论基础。
分子细胞卓越中心童欣媛博士为该论文的第一作者,季红斌研究员和上海肺科医院张鹏教授为该论文的共同通讯作者。工作得到复旦大学附属肿瘤医院陈海泉教授,浙江大学肖磊教授和上海交通大学高维强教授的大力支持,国家基金委、科技部、中科院,上海市肿瘤研究所等经费支持以及中国科学院分子细胞卓越中心动物平台和细胞分析技术平台的技术支持。
文章链接:https://www.embopress.org/doi/full/10.15252/emmm.202012627
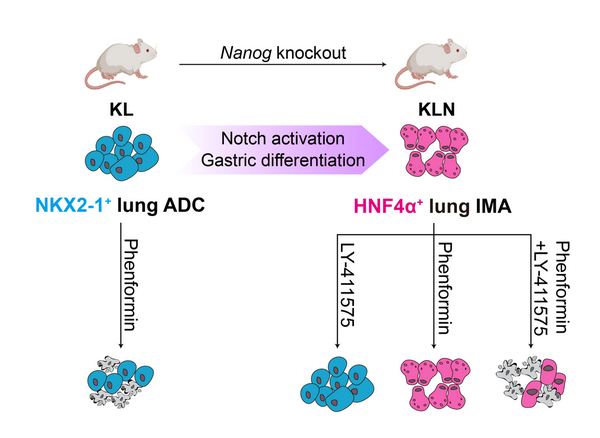
粘液型肺腺癌发病新机制模式图