5月16日,国际学术期刊Cell Chemical Biology在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)许琛琦研究组联合上海科技大学王皞鹏研究组与中国科学院生物物理所娄继忠研究组的最新合作研究成果:“Transient hydroxycholesterol treatment restrains TCR signaling to promote long-term immunity”(Featured Article)。该研究发现天然的甾醇代谢物7a-羟基胆固醇(7a-hydroxycholesterol,7a-HC)可以直接抑制TCR(T Cell Receptor)信号转导;利用该功能,作者证明7a-HC短期处理能降低TCR-T细胞基底信号,增加记忆细胞比例,从而提高免疫治疗的长效性。
胆固醇分子可以在多个位点被氧化,产生多种羟基胆固醇(氧化型胆固醇)。胆固醇可以增强CD8 T细胞免疫功能。羟基胆固醇则具有明显的免疫抑制功能,在肿瘤微环境中抑制正常的T细胞免疫应答反应(Yang et al., Nature 2016; Yan et al., Cancer Cell 2023)。然而免疫系统是一个阴阳平衡的系统,在合适的场景下可以将不利因素转化为有利因素,产生新的免疫治疗策略。
TCR/CD3复合物中的CD3ε亚基具有近膜正电残基富集区(Juxtamembrane Basic residue Rich Sequence, JM-BRS),能够与细胞质膜的负电磷脂发生静电相互作用,使得JM-BRS和临近的酪氨酸信号模体ITAM插入到膜中,从而限制了JM-BRS对Lck激酶的招募以及Lck对Immunoreceptor Tyrosine-based Activation Motif (ITAM)的磷酸化(Xu et al., Cell 2008; Shi et al., Nature 2013; Guo et al., Cell Res 2017; Li et al., PNAS 2017; Chen et al., PNAS 2023)。由于7a-HC具有3位和7位两个羟基,在细胞膜中可以削弱细胞膜脂质分子的排列致密性,使得细胞膜结构变得松散,由此帮助CD3ε胞内区更好地插入膜中,进而抑制了TCR信号转导。TCR信号是个双刃剑,一方面会引发T细胞活化与增殖,使其获得效应功能;但同时也会加速T细胞的终端分化从而削弱T细胞记忆性。因此TCR信号需要被控制在合适的水平,从而获得足够的T细胞效应功能且同时维持一定的干性,这样才能产生充分且长效的T细胞免疫反应。基于7a-HC的TCR信号抑制功能,研究团队在TCR-T细胞的体外扩增阶段进行了数次7a-HC短期处理(每次20分钟),可以明显地抑制T细胞的基底信号,并明显地增加记忆性T细胞的比例。7a-HC处理后的TCR-T细胞在长期肿瘤杀伤中具有明显的优势,该优势在动物模型中体现为更好的肿瘤控制功能。该研究由此发现了TCR信号的新调控机制,并且基于此提出了TCR-T细胞治疗的新策略。
分子细胞卓越中心博士研究生任正旭、上海科技大学博士研究生王琨、中国科学院生物物理所副研究员张勇为该论文的共同第一作者。分子细胞卓越中心研究员许琛琦、上海科技大学研究员王皞鹏以及中国科学院生物物理所研究员娄继忠为该论文的共同通讯作者。该项工作得到国家自然科学基金委员会、上海市科委、科技部、中国科学院等项目的资助,以及分子细胞卓越中心分子生物学技术平台、细胞分析技术平台的帮助与支持。
文章链接:https://www.sciencedirect.com/science/article/pii/S2451945624001673
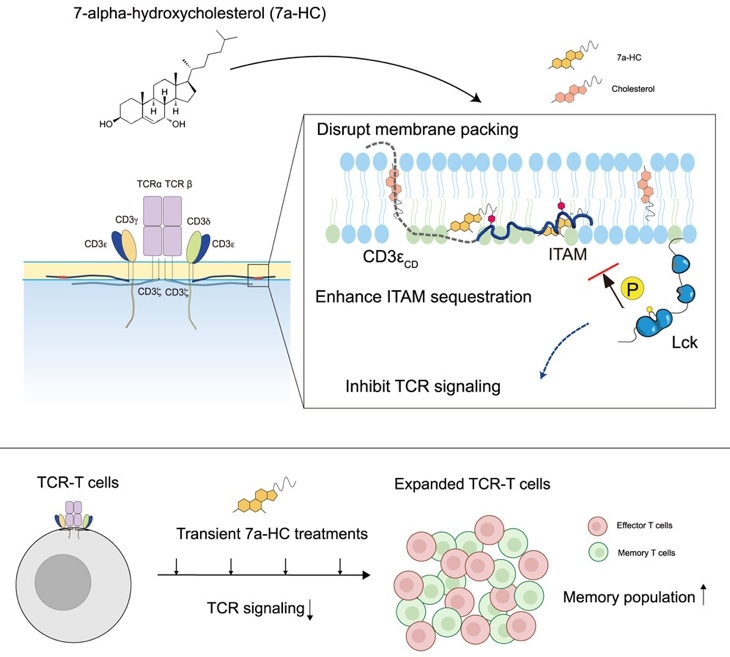
瞬时7a-羟基胆固醇处理增加TCR-T细胞的记忆群体,促进长期免疫功能