10月28日,中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)陈玲玲研究员受邀在国际学术期刊Nature Biomedical Engineering上发表了题为:"Expanded toolkits of RNA circularization”的科学评述(News&views),对同期发表在该期刊上题为:"Robust genome and cell engineering via in vitro and in situ circularized RNAs”的研究进行了点评。
RNA疗法在临床疾病治疗中具有巨大应用前景。近年来,一类单链、共价且具有闭环结构的RNA分子——环形RNA被发现普遍存在于真核细胞中,为RNA应用注入新的活力。相较于线性RNA,环形RNA具有高稳定性、特殊折叠和低免疫原性等优势(Cell Rep 2016;Cell 2019;Mol Cell 2022),为新型RNA适配体、蛋白质替代治疗、基因编辑等生物医学应用提供了潜在的改造空间和应用价值。然而,开发简单和规模化的方法以实现高效制备低免疫原性且具有长效表达能力的环形RNA,对未来基于环形RNA的治疗具有重要意义。
体外条件下,基于重组内含子-外显子(permuted intron–exon, PIE)的策略,自剪接I型内含子常用于合成环形RNA(NAR 1992;Mol Cell 2018;NBT 2024)。此外,Tornodo系统(twister-optimized RNA for durable overexpression)被报道用于细胞或在体环境中,利用广泛存在的RtcB连接酶产生环形RNA(NBT 2019)。基于上述研究,在同期的Nature Biomedical Engineering上,来自University of California San Diego的Prashant Mali团队发表了两种优化环形RNA生成的方法:基于PIE的体外环化ocRNA(outside-developed circular RNAs)和基于Tornodo的胞内环化icRNA(inside-developed circular RNAs)。随后,该团队将ocRNA和icRNA应用于干细胞分化工程和细胞基因组编辑工程,并开发了蛋白质去免疫原性的工程改造方法以筛选Cas9变体,还将这些变体以ocRNA/icRNA的形式递送,用于基因组编辑。
陈玲玲研究员的特邀专评详细论述了ocRNA和icRNA的成环过程。 ocRNA经过Twister核酶自我切割去除具有免疫原性的5'磷酸基团,通过两端互补序列靠近形成茎环结构,由自催化II型内含子发生剪接产生。与ocRNA不同的是,icRNA不含有自剪接序列,在细胞内通过RtcB连接酶将邻近的5'和3'末端通过羟基和2',3'-环状磷酸连接产生。在环形RNA应用方面,陈玲玲研究员对ocRNA和icRNA的成环效率、外源引入序列的安全性提出了新的问题和展望。陈玲玲研究团队长期致力于非编码RNA生物学研究,聚焦长非编码RNA新家族和功能的发现、环形RNA加工与功能解析等,推动了RNA作用机制与应用领域的研究进展。
分子细胞卓越中心博士后王潇和助理研究员黄友葵为该论文共同第一作者,陈玲玲研究员为该论文通讯作者。
文章链接:https://www.nature.com/articles/s41551-024-01262-y
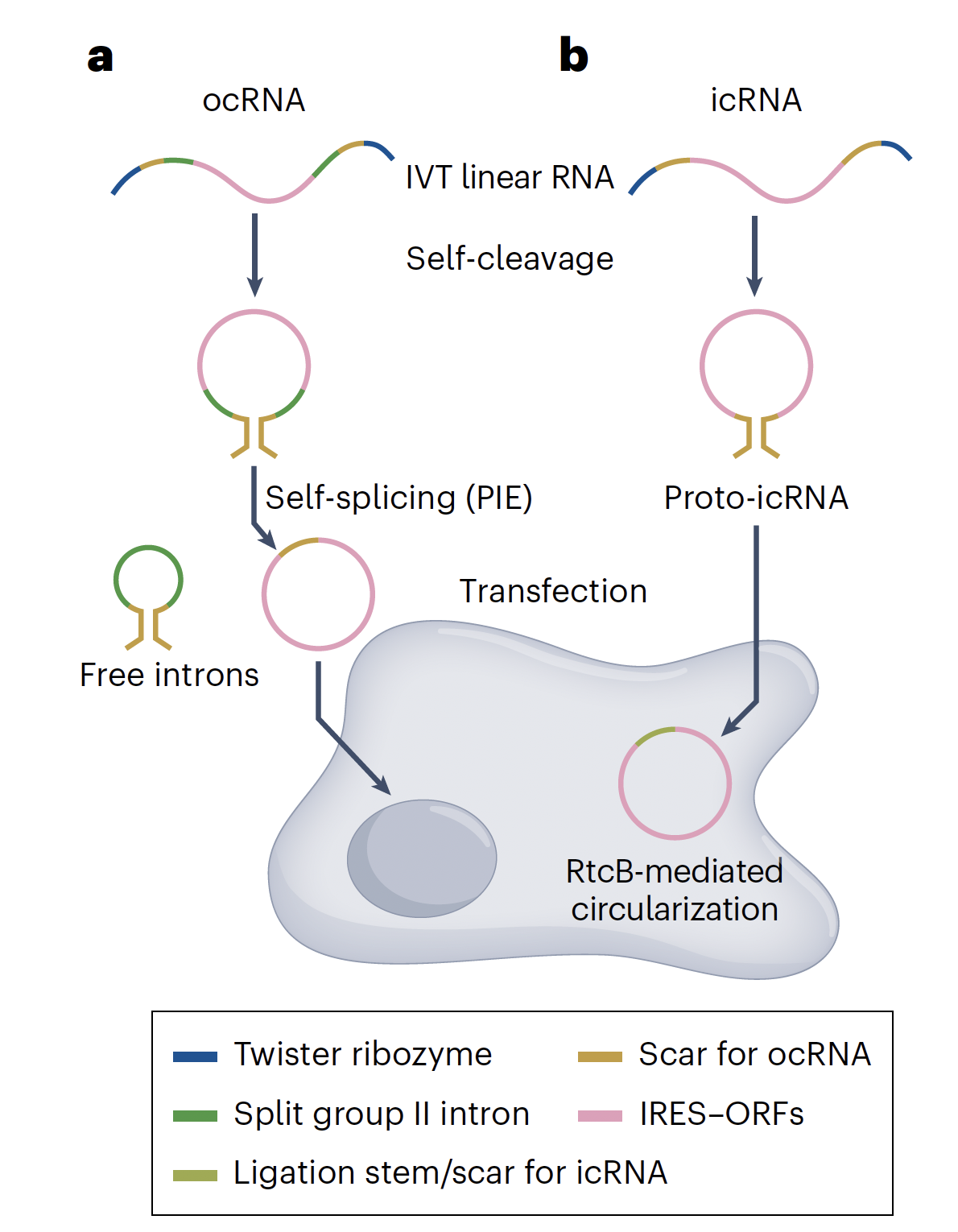
两种环形RNA环化策略