3月31日,国际学术期刊 Nature Biotechnology 在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)陈玲玲研究组的研究成果:“Circular RNA aptamers targeting neuroinflammation ameliorate Alzheimer’s disease phenotypes in mouse models”。该研究揭示了双链RNA依赖的蛋白激酶R(Protein Kinase R, PKR)在阿尔茨海默病(Alzheimer’s disease, AD)发生与进展过程中异常激活的分子病理特征,并创新性地开发了一种基于具有分子内短双链结构环形RNA(short double-stranded region-containing circular RNAs, ds-cRNA)抑制PKR异常激活的策略,从而缓解AD症状,为临床治疗提供了新的思路。
AD是一种以淀粉样蛋白(Aβ)沉积、Tau蛋白过度磷酸化及神经炎症为主要特征的神经退行性疾病。现有的治疗策略主要聚焦于Aβ斑块的清除,针对神经炎症的干预手段仍然有限。研究发现,PKR在AD患者及AD小鼠模型中呈异常激活状态,并与神经炎症及神经元损失密切相关。然而,传统的PKR小分子抑制剂因特异性较差、毒副作用高,难以在临床推广应用。前期研究表明,ds-cRNA可与PKR结合并抑制其异常激活,显示出其作为新型RNA疗法用于AD治疗的潜力。
陈玲玲团队的前期研究发现,含有 16-26bp 不完美 RNA 双链结构的环形 RNA(ds-cRNA)能够结合 PKR 并抑制其激活(Cell, 2019; Molecular Cell, 2022)。体外合成的 ds-cRNA 经纳米颗粒包裹递送后,可有效抑制银屑病模型小鼠的炎症反应并改善其皮损表型(Nature Biotechnology, 2024),验证了 ds-cRNA 在体内递送的安全性和有效性。
在本研究中,研究团队利用两种不同小鼠模型——5×FAD(以Aβ沉积为主要病理特征)和PS19(以Tau蛋白过度磷酸化为主要病理特征)——系统分析了PKR活性的动态变化。结果表明,随着疾病进展,PKR的磷酸化水平显著升高,并与神经炎症及AD病理表现呈正相关。值得注意的是,PKR基因敲除可显著改善小鼠的空间记忆能力。此外,与传统的小分子抑制剂C16相比,ds-cRNA能够高效结合PKR的双链RNA结合域,特异性抑制PKR的异常激活,且未表现出显著毒性。
研究团队进一步通过腺相关病毒(AAV)介导的递送方式,将ds-cRNA靶向表达于神经元和小胶质细胞,发现海马区域的Aβ斑块及磷酸化Tau蛋白沉积显著减少,神经元损失降低约2倍。单次给药后,治疗效果可持续至少6个月。此外,在AD早期及晚期模型中,ds-cRNA治疗均能显著改善小鼠的空间记忆能力。RNA测序分析显示,ds-cRNA通过抑制PKR激活,降低小胶质细胞的炎症通路,同时恢复突触功能相关基因的表达,从而缓解神经炎症并改善AD病理表型(图1)。
综上,该研究阐明了PKR异常激活在AD病理中的关键作用,并验证了ds-cRNA作为新型RNA疗法的潜在应用价值。通过靶向抑制PKR的异常激活,该策略有效缓解了神经炎症,并改善了AD的病理表型及认知功能,为AD的RNA治疗提供了新的策略,展现出其潜在的临床应用前景。
分子细胞卓越中心冯昕博士和姜博文博士为该论文的共同第一作者,陈玲玲研究员为该论文的通讯作者。复旦大学生物医学研究院杨力研究员对该项工作给予了大力支持。该项工作获得国家自然科学基金、科技部、中国科学院、上海市科委、上海自然科学研究院以及新基石科学基金会的支持,并获得分子细胞科学卓越创新中心分子生物学技术平台、细胞分析技术平台和动物实验技术平台的帮助与支持。
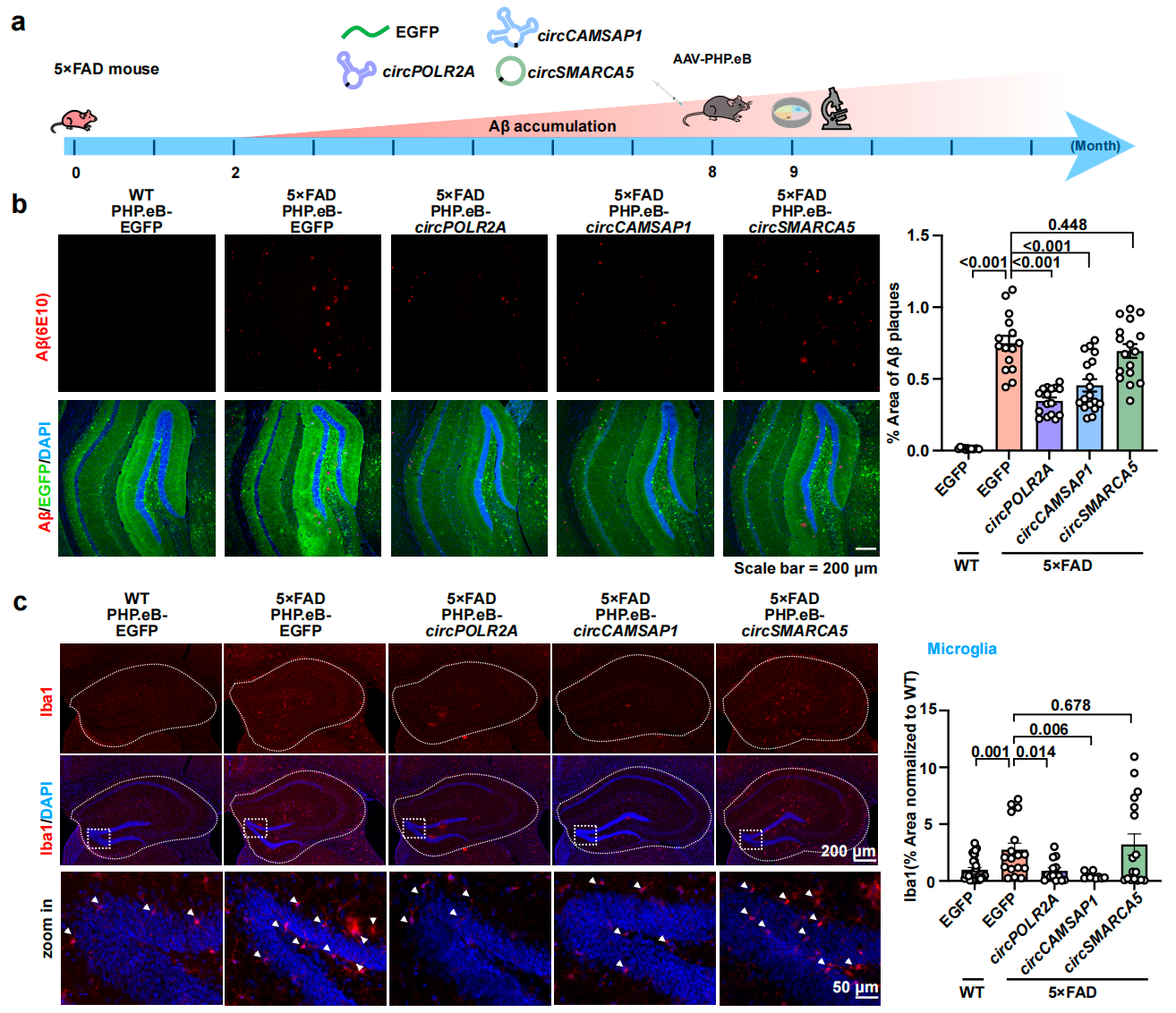
图1. AAV递送的ds-cRNA在5xFAD小鼠海马组织中减少Aβ斑沉积,抑制胶质细胞增殖。
文章链接:https://www.nature.com/articles/s41587-025-02624-w