7月23日,国际学术期刊Nature在线发表中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)陈玲玲研究员团队的最新研究成果,题为:“Pre-rRNA spatial distribution and functional organisation of the nucleolus”。该研究系统解析了构成核糖体大小亚基的rRNA前体(pre-rRNA)在核仁中的动态成熟过程,发现了核糖体小亚基(SSU)pre-rRNA的加工效率直接调控核仁内层结构的稳定性,并提出pre-rRNA加工的时空分布模型,在多层核仁形成和进化中发挥关键作用。
核仁是真核细胞中合成核糖体RNA(ribosomal RNA, rRNA)的核心场所,其空间结构复杂且高度动态。核仁由多个不同的区室在三维空间中嵌套而成,从内向外依次包括:纤维中心(Fibrillar Center, FC)、致密纤维组分(Dense Fibrillar Component, DFC)、致密纤维组分外侧区域(periphery of DFC, PDFC)和颗粒区(Granular Component, GC)。这些区室各司其职,协同完成核糖体前体 RNA (pre-rRNA)的转录、加工修饰及核糖体亚基的组装等关键步骤。其高效、有序的运行对维持细胞正常生命活动至关重要。但pre-rRNA复杂的加工成熟过程是如何在核仁高级结构中完成的以及核仁的“结构-功能”关系尚不清楚。
陈玲玲研究组长期致力于lncRNA代谢与功能的研究。围绕前期报道的两端由小核仁RNA保护的长非编码RNA SLERT,首次将超高分辨率成像技术应用于核仁研究,揭示了SLERT精准定位于DFC层,作为超低剂量“分子伴侣”调控效应蛋白质聚集,促进RNA聚合酶I转录和rRNA合成;解析了核仁的精细亚结构,提出pre-rRNA 5′端定向转运促进DFC层组装的新机制,发现了核仁新亚结构层PDFC,阐明其在pre-rRNA 3′端成熟中的关键作用,更新核仁“经典三层结构”为“四层结构”模型,深入拓展了对核仁“结构-功能”关系的理解。
在该研究中,研究人员通过整合点击化学和脉冲标记、单分子RNA成像(smFISH)、高分辨率成像和定量质谱分析等多种技术手段,从空间和时间两个维度系统解析了pre-rRNA的分布与加工轨迹。研究发现,小亚基(SSU)pre-rRNA主要分布于核仁内层的FC至PDFC区域,其主要加工过程可在标记早期(0–30分钟)完成;而大亚基(LSU)pre-rRNA则富集于PDFC至GC区域,加工逐步在标记晚期(30–60分钟)完成,揭示了核糖体大小亚基前体RNA在核仁中加工的时空分离机制。
Pre-rRNA这种时空分离的加工模式具有重要意义。由于rRNA的生成速率与细胞的生长需求密切相关,研究人员对比了不同增殖速率细胞中核仁结构与pre-rRNA空间分布和加工动力学的差异。在增殖缓慢的细胞中,FC–DFC单元呈现数量减少、体积增大的特征,SSU pre-rRNA加工效率降低,且在核仁内出现积聚, 向核仁外层区域的迁移受阻。研究人员提出“FC/DFC相对界面面积”作为几何参数,定量描述结构变化。发现FC/DFC相对界面面积与SSU pre-rRNA的加工速率高度相关。提示SSU pre-rRNA的加工与核仁内层FC-DFC结构存在密切的调控关系。
为进一步探索pre-rRNA加工过程与核仁结构之间的调控机制,研究人员采用靶向pre-rRNA 加工位点的反义寡核苷酸(ASO),特异性阻断其加工过程。实验结果显示,SSU加工阻断不仅会导致SSU pre-rRNA在核仁中异常积聚和定位偏移,还会引起FC-DFC结构膨胀甚至破裂,FC/DFC相对界面面积显著减少,重现了低增殖状态细胞中观察到的核仁结构变化。这些发现表明,FC-DFC单元不仅是SSU pre-rRNA加工的主要场所,其三维结构的稳定性也依赖于加工动态活动本身。Pre-rRNA加工与核仁结构之间形成相互协同调控的关系。这一发现为理解核仁亚结构的形成机制及空间功能分化提供了新的视角,也为在调控核糖体生成以及细胞增殖方面的靶向干预提供了理论基础。
在进化过程中,低等无羊膜动物(如斑马鱼)的核仁仅由Fibrillar zone (FZ)和Granular zone (GZ)两个区域组成,内层的FZ区域不会分离形成FC-DFC双层结构。核仁内层区域是SSU pre-rRNA的核心分布区域,这提示多层核仁结构的出现可能与pre-rRNA的加工效率相关。研究人员对比了多层结构核仁与双层结构核仁在pre-rRNA加工效率上的差异。结果显示,多层结构核仁中pre-rRNA的向外扩散速率数倍于两层结构核仁,表明核仁高级结构的出现可能在进化过程中赋予了细胞更高效的核糖体合成能力,从而更好地适应不同的生理与增殖需求。
该研究基于实际的细胞生理状态,建立了pre-rRNA加工功能与核仁多层结构之间的直接关联,深入揭示了核仁“结构–功能”的协同调控机制,拓展了对核仁空间功能组织模式的理解,为进一步探究核糖体相关疾病的发生机制及开发潜在干预策略提供了基础。
分子细胞卓越中心陈玲玲研究组博士生潘宇航、博士后单琳和复旦大学生物医学研究院博士生张宇瑶为该论文的共同第一作者。分子细胞卓越中心陈玲玲研究员为该论文的唯一通讯作者。该工作得到复旦大学生物医学研究院/复旦大学附属儿科医院杨力研究员、分子细胞卓越中心细胞分析技术平台和斑马鱼技术平台、以及中国科学院、科技部、上海市尚思科学研究院和新基石科学基金会的大力支持。
文章链接:https://www.nature.com/articles/s41586-025-09412-1
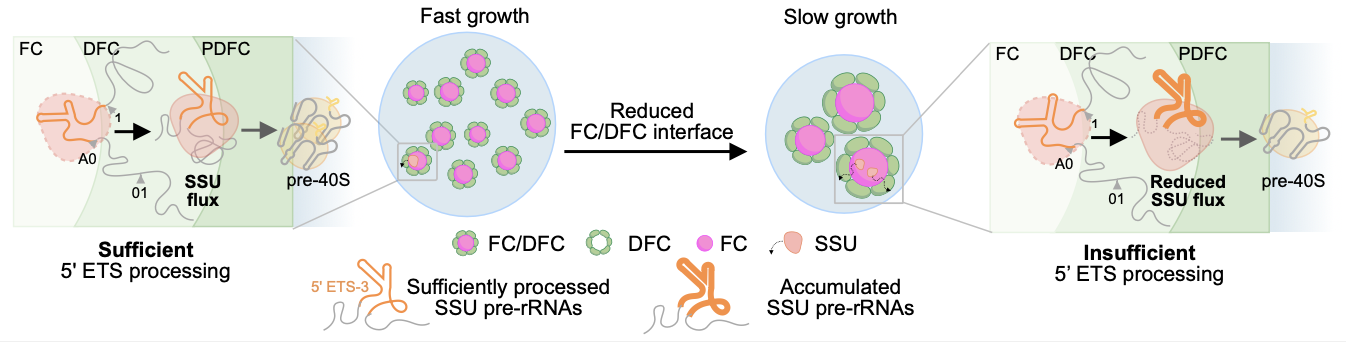
pre-rRNA 加工与核仁高级结构协同调控以响应不同细胞状态需求