8月13日,国际学术期刊Cell Stem Cell在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)高栋研究组、上海长海医院金钢团队、中国科学院上海药物研究所周虎研究组、上海交通大学人工智能学院陈洛南研究组以及中国科学院数学与系统科学研究院王勇研究组的合作研究成果:“A pancreatic cancer organoid biobank links multi-omics signatures to therapeutic response and clinical evaluation of statin combination therapy”。研究团队构建了目前规模最大、覆盖病理亚型最全面的胰腺癌类器官库,并通过多组学和药物敏感性整合分析,解析了胰腺癌化疗耐药机制,鉴定出多个具有临床转化价值的新型药敏标志物与治疗靶点。基于这些发现,团队开展了他汀类药物联合标准化疗的II期临床实验,研究结果证实他汀可以显著提高胰腺癌患者的化疗敏感性,为晚期胰腺癌的临床干预提供了突破性的治疗前景。
胰腺癌类器官库构建与特征描绘
胰腺导管腺癌(PDAC)是最恶性的实体肿瘤,五年生存率不足12%。化疗是PDAC临床治疗的基石,但绝大多数患者对化疗反应极差。为攻克这一临床难题,研究团队构建了239例PDAC类器官、21例其他病理亚型类器官(包括IPMN、ASC、ACC、SPT)以及18例胰腺正常导管类器官。研究团队对类器官进行了多组学检测(包括WGS,RNA-seq,ATAC-seq,Proteome,Phosphoproteome,Glycoproteome),并开展了超过100种药物和放疗的敏感性检测。
开发HNetDig探索致癌驱动突变
研究团队开发了驱动突变识别工具“HNetDig”,在全基因组范围内精准识别编码区与非编码区的功能突变。利用该工具,研究人员在PDAC中识别出6个新的编码驱动突变和35个非编码驱动突变,这些突变富集于进化保守的启动子或增强子区域。团队通过CRISPR/Cas9编辑类器官的非编码区,证实了非编码突变在促进PDAC进展中的驱动功能。
多维组学联合药敏揭示治疗靶点和药敏标志物
基于OncoKB和CGI数据库提供的泛癌靶向治疗靶点,研究团队发现79.6%的胰腺癌类器官携带潜在可被靶向的基因变异(AGVs),涉及PI3K、MAPK、DNA损伤修复等关键信号通路。研究团队进一步开展了100种靶向药物、临床常用化疗药物以及放射敏感性的大规模筛选,发现38%的AGV-Drug组合在体外类器官药敏实验中得到验证。更重要的是,团队利用ANOVA和LOBICO方法,鉴定出2794个与药物反应显著相关的分子特征(multi-omic features, MOFs),322个与放射敏感性相关的MOFs,涵盖编码突变、非编码突变、蛋白及RNA表达水平变化、表观修饰等多维组学信息,建立了胰腺癌药物反应与分子特征之间的全景图谱。这些MOFs为胰腺癌的临床治疗提供了新型药敏标志物与治疗靶点。
他汀诱导胰腺癌化疗敏感性
研究团队发现蛋白糖基化水平和胆固醇代谢水平升高是胰腺癌对化疗耐药的重要标志。同时,团队发现他汀类药物可选择性抑制化疗耐药型类器官的生长。进一步机制研究表明,他汀类药物通过抑制胆固醇代谢和糖基化通路,显著下调EMT相关基因,进而提高类器官化疗的敏感性。研究团队进一步利用原位移植和皮下移植模型,证实了他汀与化疗联用在体内协同抑制肿瘤的生长。
临床实验证实他汀提升晚期胰腺癌病人化疗效果
基于前期基础研究成果,研究团队开展了一项II期临床试验(NCT06241352),招募42例化疗平台期的晚期PDAC患者,在标准化疗基础上联合应用阿托伐他汀(80mg/天)。在37名完成随访的患者中,有26人(70.3%)的肿瘤标志物(CA19-9或CEA)在联合用药1个月后下降超过20%。截至随访更新日期,平均缓解维持时间达62天以上。影像结果表明,大部分胰腺癌患者肿瘤体积也显著缩小。这一结果首次证实了他汀药物对耐药PDAC的治疗潜力,为化疗耐药胰腺癌患者提供了新的治疗机会。研究团队后续将进行多中心随机对照实验,进一步证实他汀在诱导胰腺癌病人化疗敏感性中的作用。
中国科学院分子细胞科学卓越创新中心李允广副研究员、上海市第一人民医院唐诗婕副研究员、长海医院王欢主治医师、郭世伟副教授、中国科学院上海药物研究所朱洪文副研究员、中国科学院数学与系统科学研究院路雨润博士、上海市第一人民医院张晔晗博士后为该论文的共同第一作者。中国科学院分子细胞科学卓越创新中心高栋研究员、长海医院金钢教授、中国科学院上海药物研究所周虎研究员、上海交通大学人工智能学院陈洛南研究员和中国科学院数学与系统科学研究院王勇研究员为该论文的共同通讯作者。该项研究工作得到了国家自然科学基金、中国科学院战略性先导科技专项、尚思探索学者基金会、上海市科学技术委员会等资助。该项研究工作得到了分子细胞卓越中心细胞生物学技术平台、化学生物学技术平台和动物实验技术平台的支持。
文章链接:https://doi.org/10.1016/j.stem.2025.07.008
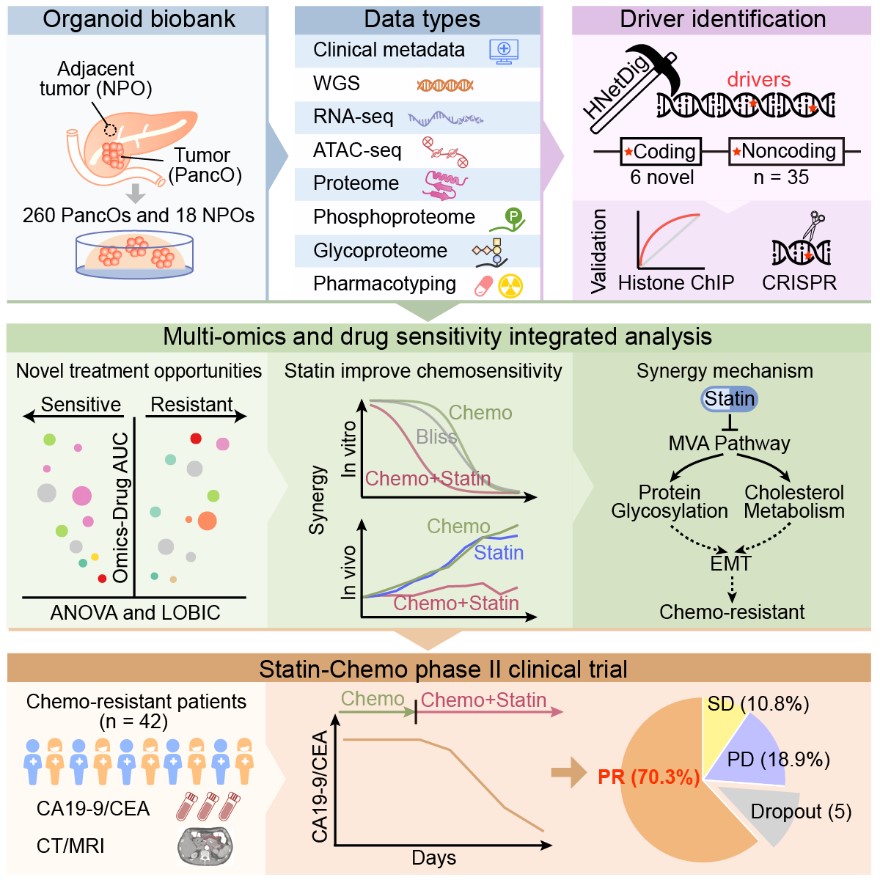
类器官库揭示他汀联合治疗的分子机制与临床潜力