2月27日,国际学术期刊 Nucleic Acids Research 在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)王露研究组与吴薇研究组的最新合作研究成果:“A de novo H3.2K9me2 deposition pathway establishes heterochromatin for suppressing transposon mobilization during fly somatic development”。该研究以果蝇直肠发育为模型,系统揭示了DNA复制偶联的H3.2K9me2分子伴侣通路在体细胞发育过程中建立功能性异染色质、抑制转座子活化及转座的关键作用。
转座子广泛存在于真核生物基因组中,其异常激活和转座可引发基因组不稳定,甚至导致发育异常、衰老相关改变及遗传疾病。因此,细胞需要依赖DNA甲基化和组蛋白翻译后修饰等表观遗传机制对转座子实施严格抑制。既往研究表明,组蛋白H3不同变体及其伴侣蛋白在染色质组装和异染色质维持中发挥重要作用。其中,DNA复制偶联(DNA synthesis-coupled,DSC)途径主要负责经典H3.2的装配,而DNA复制非依赖(DNA synthesis-independent,DSI)途径则主要介导H3.3的装配。然而,在体细胞发育过程中,究竟哪一条通路在转座子抑制中发挥主导作用,以及不同H3变体修饰如何协同建立异染色质,仍有待深入阐明。
本研究中,研究人员利用果蝇直肠这一可监测体细胞转座事件的模型体系,结合单细胞水平分辨率的转座报告系统,对DSC与DSI两类组蛋白H3分子伴侣通路在发育过程中的作用进行了系统比较。结果发现,敲低DSC通路中的关键伴侣蛋白可显著增强逆转座子激活和转座;相比之下,干扰DSI-H3.3伴侣通路仅产生较为有限的影响。进一步研究表明,在果蝇直肠发育和再生过程中,DSC通路在转座子沉默中发挥主导作用。
进一步研究表明,不同的组蛋白变体及其翻译后修饰在染色质上的定位存在明显偏好性,其中H3.2及其所携带的K9me2修饰在异染色质区域显著富集,而H3.3则主要分布在常染色质位点。机制研究显示,DSC伴侣蛋白能够在DNA复制时优先将组蛋白变体H3.2递送至异染色质区域,并特异性促进H3.2第9位赖氨酸二甲基化(H3.2K9me2)的建立。研究发现,CAF-1复合体亚基Caf1-180可直接与组蛋白甲基转移酶G9a相互作用,并将其募集至异染色质区域,从而催化H3.2K9me2的形成。与之相对,另一条DSI通路则主要介导H3.3K9me3的形成。该结果表明,不同H3变体及其修饰并非简单冗余,而是通过各自分工共同参与异染色质的组织与建立。
值得注意的是,研究人员进一步发现,当DSC-H3.2K9me2通路受损时,DSI途径可在一定程度上增加H3.3K9me3在转座子位点的建立,表现出一定的补偿效应。然而,这种补偿并不足以重建发育过程中所需的功能性异染色质,转座子仍会发生显著激活。这提示,H3.2K9me2与H3.3K9me3之间虽然存在动态平衡与交叉调控,但二者在生理功能上具有不可替代的特异性,其中H3.2K9me2在建立即时有效的转座子沉默状态中尤为关键。
综上,该研究揭示了体细胞发育过程中一条全新的de novo H3.2K9me2分子伴侣通路,阐明了DNA复制偶联的组蛋白装配机制如何通过募集G9a建立异染色质并抑制转座子转座。该工作不仅加深了对组蛋白变体修饰与异染色质建立机制的理解,也为认识细胞如何在发育过程中维持基因组稳定性提供了新的理论框架。
分子细胞卓越中心王露研究员和吴薇研究员为论文共同通讯作者。王露研究组博士研究生罗依妮、邓雅姿和吴薇研究组博士研究生梁羽为共同第一作者。该课题获得了中国科学院战略性先导科技专项、国家重点研发计划、国家自然科学基金、上海市自然科学基金、中国科学院国际伙伴计划、上海市科技重大项目及上海市启明星计划等项目资助,并获得了清华大学果蝇中心倪建泉博士、分子细胞卓越中心果蝇资源与技术平台、中南大学袁凯老师、哈佛医学院Norbert Perrimon博士、奥地利维也纳生物中心Julius Brennecke教授以及VDRC 和BDSC等帮助。
文章链接:https://doi.org/10.1093/nar/gkag146
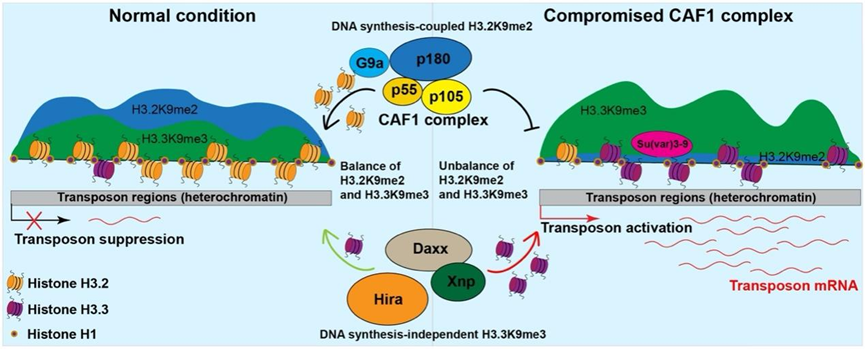
果蝇体细胞发育中H3.2K9me2与H3.3K9me3协同维持转座子沉默的工作模型