3月26日,国际学术期刊Cancer Cell发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)惠利健组与中国科学院营养与健康研究所李虹研究员、中山医院病理科纪元教授的最新研究成果:“Molecular insights into early malignant transition of hepatocellular carcinoma”。该研究全球首次系统解析了肝癌极早期恶变的原因,为肝癌早期预警与干预提供了全新的理论依据。
癌变从来不是一蹴而就的突变,而是一场循序渐进的“恶变之旅”。其中,癌前病变向早期癌症的转变,更是整个癌变进程里最关键的核心环节。这一节点直接关系临床决策:对于癌前结节通常以随访监测为主,而一旦确诊为恶性肿瘤则需立即干预。因此,阐明该转变过程的分子机制及其特征,对于实现癌症的早期预防与精准治疗具有重要意义。
然而,既往研究多基于缺乏演化关联的癌前病变与肿瘤样本,通过统计推断分析恶性转变相关的遗传及微环境变化,存在明显局限。一方面,多数纳入的癌前病变缺乏实际癌变潜力,参考价值有限;另一方面,即便通过手术取得小体积肿瘤样本,此时癌细胞的恶性特征已经完全成型,难以捕捉恶性转变发生的极早期临界状态。此外,肿瘤微环境是动态变化的,用演化毫无关联的样本进行分析,会大幅干扰判断,无法准确锁定恶性转化过程中微环境的真实变化规律。
相比之下,采用具有明确演化关联的配对癌前与肿瘤样本,才能为解析恶性转变的机制提供确定性证据。其中,伴早期癌的“结节内结节”型不典型增生结节(Dysplastic nodule, DN)是理想的研究对象。这类病变能够精准定格恶性转变的关键节点,同时捕捉癌前与早期癌恶性特征,是界定驱动恶性转变的关键遗传变异及微环境改变的理想载体。然而,该类病变在临床中极为罕见,由于恶性细胞增殖迅速,两类病灶共存的时间窗口极短,这类样本获取难度极大,成为制约该领域研究的重要瓶颈。
为攻克人肝细胞癌(HCC)早期恶性转变的分子机制这一科研难题,研究团队与国内3家大型肝癌中心合作,历时9年深耕,从逾44000份FFPE人肝癌手术样本中严格筛选,最终成功获取17例珍贵的“结节内结节”临床样本,为破解肝癌早期恶性转变谜团奠定了核心样本基础。研究团队针对这批配对的高危不典型增生结节(Cancer-prone DN)及其内部的极早期肝细胞癌(very early HCC, veHCC),开展了系统性的基因组与免疫图谱全景分析。
研究结果显示,82%的cancer-prone DN存在TERT激活变异,提示TERT异常是肝癌恶变的前置风险因素。令人意外的是,veHCC的SNV负荷与配对DN无显著差异,仅29%的veHCC积累了新的SNV诱导的癌症功能基因(Cancer functional gene, CFG)变异,与之形成鲜明对比的是,veHCC的CNA负荷较配对DN显著升高,且83%的veHCC获得了新的CNA诱导的CFG变异,这些结果表明CNA而非SNV积累可能是驱动肝癌早期恶性转变的核心分子事件。
结合表达谱、空间转录组与原位多色染色分析,团队进一步揭示了肝癌早期恶性转变的免疫表型特征:cancer-prone DN多呈现免疫静默表型,促炎信号显著下调,免疫与基质细胞浸润水平很低,这与肝癌起源于炎症活跃微环境的传统认知不符。
发生恶性转变后,43%的veHCC形成“炎症型伴免疫逃逸”表型,免疫与基质细胞浸润显著增多,同时启动多重免疫抑制程序;而剩余veHCC则维持免疫静默的非炎症表型,且这类非炎症型veHCC的CNA负荷显著高于炎症型veHCC。
基于上述基因组与免疫图谱数据,研究团队提出肝癌早期恶性转变的“双演化路径”:一是CNA主导型进展(高CNA负荷、低免疫浸润),二是伴早期免疫逃逸的炎症型进展(低CNA负荷、高免疫浸润伴免疫抑制)。
综上所述,本研究利用“结节内结节”型配对DN与veHCC样本,整合全基因组测序、转录组、空间转录组及组织原位多色染色等多技术平台,全球首次系统解析了肝癌极早期恶性转变的分子驱动机制与免疫微环境演化规律。研究不仅明确了CNA累积而非SNV是驱动肝癌早期恶变的核心事件,鉴定出TERT异常为关键前置风险因素,更挑战了肝癌起源于炎症活跃微环境的传统认知,揭示了免疫静默-免疫逃逸的动态表型转换,并提出肝癌早期恶变的双演化路径,为肝癌的早期预警及早期免疫干预策略开发提供了全新的理论依据。
分子细胞卓越中心章正涛博士,中国科学院营养与健康研究所李虹研究员与中山医院病理科陈伶俐博士为该论文共同第一作者。惠利健研究员、李虹研究员以及中山医院病理科纪元教授为该论文的共同通讯作者。该工作得到了分子细胞卓越中心许琛琦、周金秋研究员,上海交通大学免疫所李兵教授,中国科学院生物物理所杨鹏远研究员,南开大学刘林教授以及苏州系统医学研究所李贵登研究员的指导和帮助。该工作得到了分子细胞卓越中心化学生物学技术平台、细胞分析技术平台和分子生物学技术平台的大力支持。该工作得到了基金委、科技部、上海市科委和中国科学院等项目的资助。
文章链接:https://www.cell.com/cancer-cell/fulltext/S1535-6108(26)00157-1
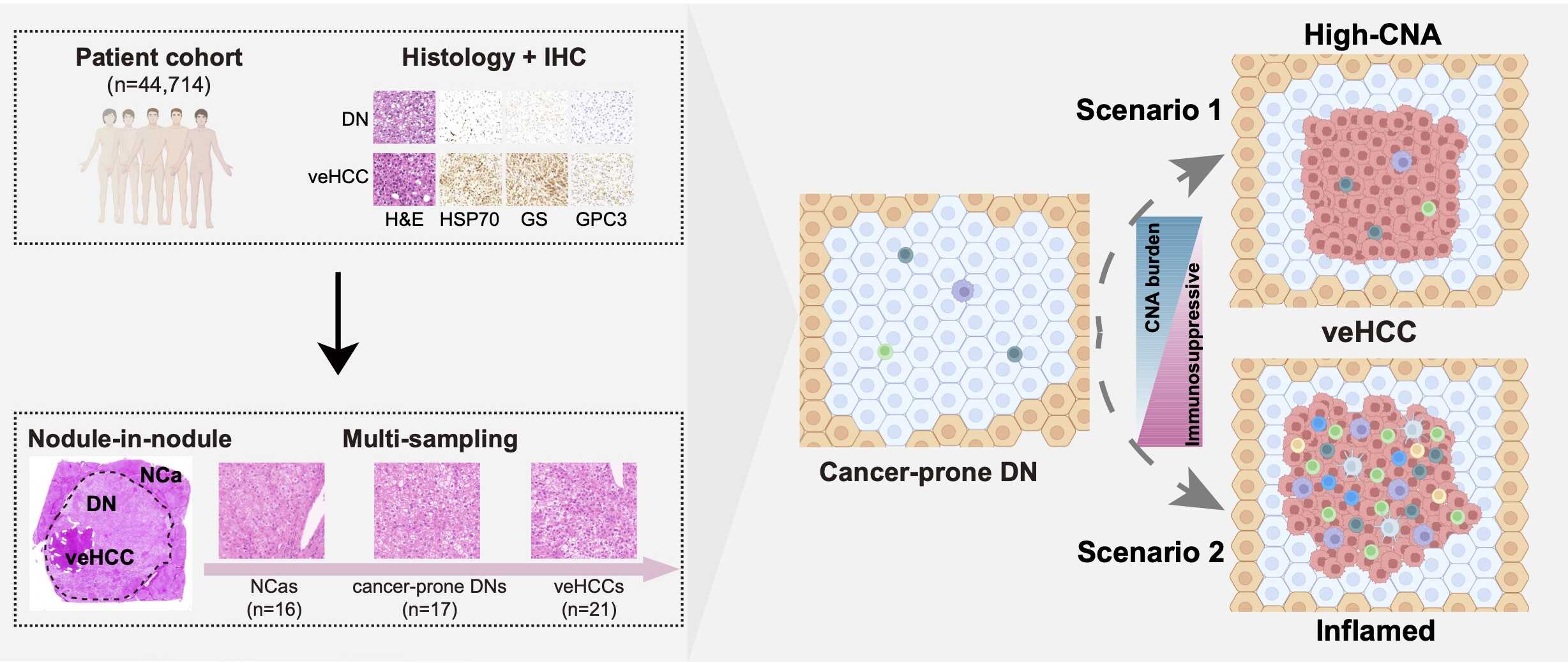
明确了肝癌早期恶性转变的基因组不稳定性与免疫逃逸的“双轨驱动”模式